94 % geringeres Herzerkrankungsrisiko! Lepodisiran von Eli Lilly senkt Risikofaktor deutlich laut seiner Phase-2-Ergebnisse!
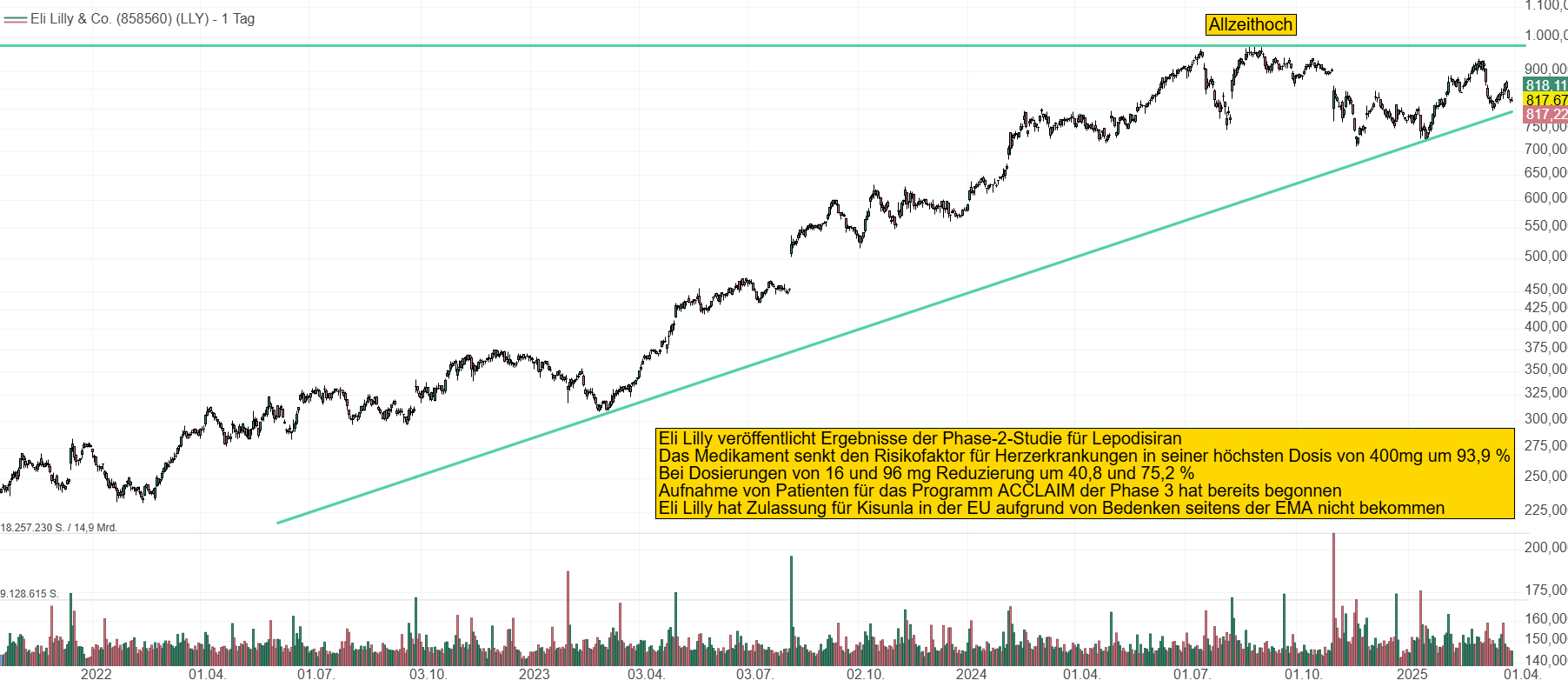
Das Pharmaunternehmen Eli Lilly and Company (LLY) hat am Sonntag, den 30. März 2025, einen Bericht über seine Ergebnisse der Phase-2-Studie für seinen siRNA-basierten Wirkstoffkandidaten Lepodisiran veröffentlicht. Laut den positiven Studienergebnissen zeigt das Medikament eine um 94 % niedrigere Konzentration eines genetisch bedingten Risikofaktors bei erwachsenen Patienten mit Herzerkrankungen, die die höchste Testdosis des Wirkstoffkandidaten verabreicht bekommen haben.
ALPACA ist eine Phase-2-Studie für sein Medikament Lepodisiran
Eli Lilly führt derzeit eine Phase-2-Studie namens ALPACA für sein Medikament Lepodisiran durch. Lepodisiran ist eine experimentelle Therapie mit siRNA (small interfering RNA) zur Senkung der Produktion von Lipoprotein(a), einem genetisch bedingten Risikofaktor für Herzerkrankungen. Das Medikament soll die Produktion von Apolipoprotein(a), einem Schlüsselbestandteil von Lp(a), hemmen. Die Forschungsstudie ALPACA ist eine randomisierte, doppelblinde, placebokontrollierte Phase-2-Studie zur Untersuchung der Wirksamkeit und Sicherheit von Lepodisiran bei Erwachsenen mit erhöhtem Lp(a)-Wert. Insgesamt haben 320 Teilnehmer an der Studie teilgenommen und erhielten zufällig entweder Placebo oder eine von drei Lepodisiran-Dosierungen zu Studienbeginn und an Tag 180. Die erhältlichen Dosierungen sind 16 mg, 96 mg und 400 mg. Eine weitere Gruppe erhielt zu Studienbeginn die Maximaldosierung von 400 mg Lepodisiran und an Tag 180 Placebo. Die Ergebnisse dieser beiden Gruppen, die jeweils 400 mg Lepodisiran erhielten, wurden für die primäre Analyse zusammengefasst. Der primäre Endpunkt war die placeboadjustierte, zeitgemittelte prozentuale Veränderung der Lp(a)-Serumkonzentration von Tag 60 bis Tag 180.
Lepodisiran mit der höchsten Konzentration senkt Risiko um 93,9 %
Ergebnisse der Phase-2-Studie ALPACA zeigten, dass Lepodisiran die Konzentration genetisch bedingter kardiovaskulärer Risikofaktoren signifikant senkte. Bei einigen Patienten blieb die langanhaltenden niedrigen Lp(a)-Werte fast 1,5 Jahre lang bestehen. Die höchste getestete Dosis betrug 400 mg und senkte den Spiegel um durchschnittlich 93,9 % und erreichte damit den primären Endpunkt. Bei Studienteilnehmern, die 16 mg bzw. 96 mg Lepodisiran einnahmen, sanken die Lp(a)-Werte während der 18-monatigen Studie um 40,8 % bzw. 75,2 %. Diese Daten wurden auf den Scientific Sessions 2025 des American College of Cardiology vorgestellt und gleichzeitig im New England Journal of Medicine veröffentlicht.
"Die Senkung des vererbten kardiovaskulären Risikos bei Patienten mit hohem Lp(a)-Spiegel war lange Zeit ein dringender Bedarf. Diese Ergebnisse geben Hoffnung auf eine langfristige, nachhaltige Behandlungsoption. Diese Daten unterstreichen Lillys Engagement für die Weiterentwicklung der genetischen Medizin, um eine der drängendsten Herausforderungen im Gesundheitswesen weltweit zu bewältigen. Wir werden den potenziellen Nutzen von Lepodisiran in der laufenden Phase-3-Studie zu kardiovaskulären Ergebnissen weiter untersuchen.", sagte Ruth Gimeno, Group Vice President für Diabetes-, Adipositas- und kardiometabolische Forschung bei Eli Lilly.
25 % der Weltbevölkerung sind von einem erhöhten Lp(a)-Wert betroffen
"Fast ein Viertel der Weltbevölkerung weist erhöhte Lp(a)-Werte auf, was ein deutlich erhöhtes Risiko für kardiovaskuläre Ereignisse wie Herzinfarkte und Schlaganfälle bedeutet. Leider gibt es keine zugelassenen cholesterinsenkenden Therapien speziell für diesen genetischen Risikofaktor, und Lebensstiländerungen wie Ernährung und Bewegung führen nicht zu einer nennenswerten Senkung. Diese signifikanten und anhaltenden Lp(a)-Senkungen sind ermutigend und deuten darauf hin, dass siRNA-Ansätze wie Lepodisiran bei Langzeitdosierung möglicherweise dauerhafte Vorteile bieten könnten." sagte Dr. Steven Nissen, Chief Academic Officer des Heart, Vascular & Thoracic Institute der Cleveland Clinic.
Mehrere sekundäre Endpunkte und Reduktionen der Lp(a-)-Werte erreicht
Lepodisiran erreichte zudem weitere sekundäre Endpunkte und zeigte Reduktionen der Lp(a)-Werte nach ein- oder zweimaliger Verabreichung jeder der drei getesteten Dosierungen über alle Zeitpunkte der fast 18-monatigen Studie hinweg. Teilnehmer, die zu Studienbeginn und an Tag 180 400 mg Lepodisiran erhielten, verzeichneten im Zeitraum von Tag 30 bis 360 eine Senkung des durchschnittlichen Lp(a)-Spiegels um 94,8 %. Dieser blieb an Tag 360 91,0 % und an Tag 540 74,2 % unter dem Ausgangswert. Zudem senke Lepodisiran den Apolipoprotein-B-Spiegel, einen separaten Cholesterin-Biomarker. Behandlungsbedingte unerwünschte Ereignisse im Zusammenhang mit dem Studienmedikament traten bei 14 % (20/141) der gepoolten 400-mg-Gruppe auf, jedoch nichts Schwerwiegendes. In der 16-mg-Dosisgruppe trat ein Todesfall aufgrund von Komplikationen einer chronischen Koronarerkrankung auf. Die Aufnahme von Patienten für sein klinisches Entwicklungsprogramm ACCLAIM-Lp(a) der Phase 3 hat bereits begonnen und soll die Wirkung von Lepodisiran auf die Verringerung kardiovaskulärer Ereignisse bei Erwachsenen mit erhöhtem Lp(a) untersuchen.
Eli Lilly erhält keine EU-Unterstützung für Alzheimer-Therapie
Die Ergebnisse der Studie mit Lepodisiran sind sehr vielversprechend, aber noch keine Garantie für eine Zulassung. Die FDA hatte eine gegen Amyloid gerichtete Therapie mit Kisunla noch im Juli zugelassen, dem Wirkstoffkandidaten von Eli Lilly zur Behandlung von Alzheimer bei Erwachsenen im Frühstadium. Nun lehnte ein Expertengremium der EU-Arzneimittelbehörde EMA die Zulassung von Kisunla (Donanemab) ab. Der Ausschuss für Humanarzneimittel (CHMP) der EMA gab eine negative Stellungnahme zur Marktzulassung von Kisunla in der EU ab und verwies auf amyloidbedingte Bildgebungsanomalien, eine potenziell tödliche Nebenwirkung im Zusammenhang mit der intravenösen Infusion. Das Nutzen-Risiko-Profil sei dadurch nicht mehr gegeben.
Bildherkunft: AdobeStock_1312639763